导读
2024年5月,Altos Labs团队在《科学》发表重磅成果:通过瞬时重编程技术,将90岁供体的细胞表观遗传年龄逆转至30岁水平,且无致瘤风险;2024年6月,张锋团队开发的“表观遗传橡皮擦”技术登上《自然·生物技术》,可完全消除细胞记忆;2024年《自然·医学》数据显示,“iPSC分化成“通用型”T细胞的技术使CAR-T制备成本从50万美元降至2万美元,且无需等待个体化制备。一个又一个关于iPSC技术突破及临床研究的消息如雨后春笋,究竟iPSC是一项怎样的技术,为什么能在生物医学领域引起研发热潮?正如诺奖得主山中伸弥所言:“iPSC的故事才刚写完序章,真正的奇迹将在未来十年降临病房”。

(图1:诺奖得主山中伸弥,图源于网络)
iPSC是诱导多能干细胞,由体细胞通过导入特定基因使体细胞重编程,具有类似胚胎干细胞的多能性细胞,具备多向分化潜能,可以分化为内、中、外三胚层的所有细胞类型,几乎涵盖人体各种组织和器官的所有细胞,可在体外长期培养并保持稳定状态。iPSC来源广泛,可从皮肤、血液等易获取的组织中提取体细胞进行重编程,且可避免免疫排斥。具有无限复制能力和较高的基因编辑效率,为个性化细胞治疗和再生医学研究提供了重要工具。
起源:一场伦理困局的破冰
2006年,日本京都大学的实验室里,47岁的山中伸弥教授盯着显微镜下的培养皿,手指微微颤抖——原本普通的小鼠皮肤细胞,竟在导入四个特殊基因后,奇迹般地“返老还童”,变成了具有无限潜力的干细胞。随后,山中伸弥团队在《细胞》杂志发表划时代成果:通过导入Oct4、Sox2、c-Myc、Klf4四个转录因子,成功将小鼠皮肤细胞重编程为具有胚胎干细胞特性的诱导多能干细胞(iPSC)。这项被称为“诱导多能干细胞(iPSC)”的发现,不仅让山中伸弥获得2012年诺贝尔生理学或医学奖,更打破了困扰科学界数十年的伦理困局——无需破坏胚胎即可获得多能干细胞。其意义堪比干细胞领域的”莱特兄弟首飞”,标志着再生医学进入全新纪元。
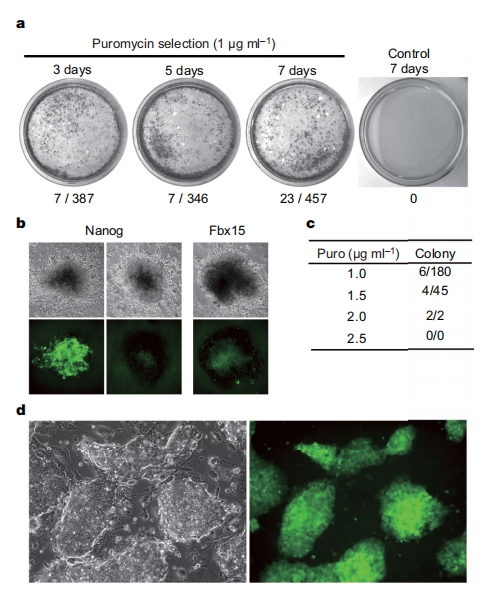
(图2:Generation of iPS cells from MEFs of Nanog-GFP-IRES-Puror transgenic mice.来源:Okita, K., Ichisaka, T., and Yamanaka, S. (2007).Generation of germline-competent induced pluripotent stem cells. Nature 448, 313-317.)
此前,人类获取干细胞的唯一途径是破坏早期胚胎,这引发了激烈的伦理争议。而iPSC技术的诞生,让普通体细胞通过基因重编程“逆生长”为干细胞,不仅避免了胚胎破坏,更让每个成年人成为自己的“干细胞银行”。当山中伸弥在2012年接过诺贝尔奖章时,评委如此评价:“他让生命时钟实现了双向转动。”
发展:从实验室到病床的二十年狂奔
iPSC的故事,是一部技术与时间赛跑的史诗。
2007年,当第一例人类皮肤细胞成功转化为iPSC时,波士顿儿童医院的走廊里,一群患有脊髓性肌萎缩症的孩子家长彻夜守候。他们知道,这种能定向分化为神经细胞的“魔法细胞”,或许能改写孩子们的生命轨迹。
技术的进化比想象中更快:2014年,日本理化研究所的高桥政代团队将iPSC分化的视网膜细胞植入失明患者眼中,让沉寂多年的视神经重新感知光明;2020年,跳动在培养皿中的iPSC心肌细胞,开始替代心力衰竭患者坏死的组织;到了2023年,3D生物打印机喷出的iPSC“生物墨水”,已在实验室里构建出具备代谢功能的微型肝脏。
在这条赛道上,中国科学家同样留下深刻印记。北京大学邓宏魁团队开发的化学小分子诱导法,让细胞重编程过程完全避开基因操作,犹如用“无痕手术”实现细胞年轻化;而中科院广州生物院的裴端卿团队,则破解了细胞“记忆擦除”的分子密码,使重编程效率提升20倍。
技术之争:四大门派的华山论剑
在这场细胞重编程的革命中,不同技术流派如同武侠世界的各大门派,各显神通,在转染效率和安全性上不断进行创新突破:
病毒载体法:用逆转录病毒将重编程基因强力注入细胞,病毒载体法转染效率高,能快速将目标基因导入体细胞。合大规模细胞重编程,可短时间内获得大量iPSC。虽效率惊人,却有基因插入突变的风险,如同武功霸道却易伤经脉。
非病毒载体法:采用游离基因载体或蛋白质直接渗透,确保细胞基因组的完整性,虽见效稍缓,却更安全可控。如质粒转染安全性高,无病毒载体的插入突变风险;mRNA转染效率较高,且转染后的基因表达迅速;蛋白质转导直接将蛋白质导入细胞,避免了基因整合问题。
小分子化合物诱导法:独辟蹊径,用维生素C、丙戊酸等小分子调控表观遗传,无需复杂的病毒载体或转染操作。不碰DNA却能唤醒细胞的潜能,安全性高,避免了基因整合带来的潜在风险。
无痕重编程法:CRISPR/Cas9可靶向特定基因位点,直接激活内源重编程因子(如Oct4、Sox2),避免外源基因随机插入导致的基因组损伤。但是该技术复杂度高,需设计特异性sgRNA,并优化递送系统(如电转、纳米颗粒),操作难度大。CRISPR可能非特异性切割非目标位点,导致基因组不稳定或意外突变。需优化递送效率、降低脱靶率,并确保基因组稳定性。
这些技术的角力与融合,正推动iPSC从精密的手工艺术,进化为标准化的生物工程。
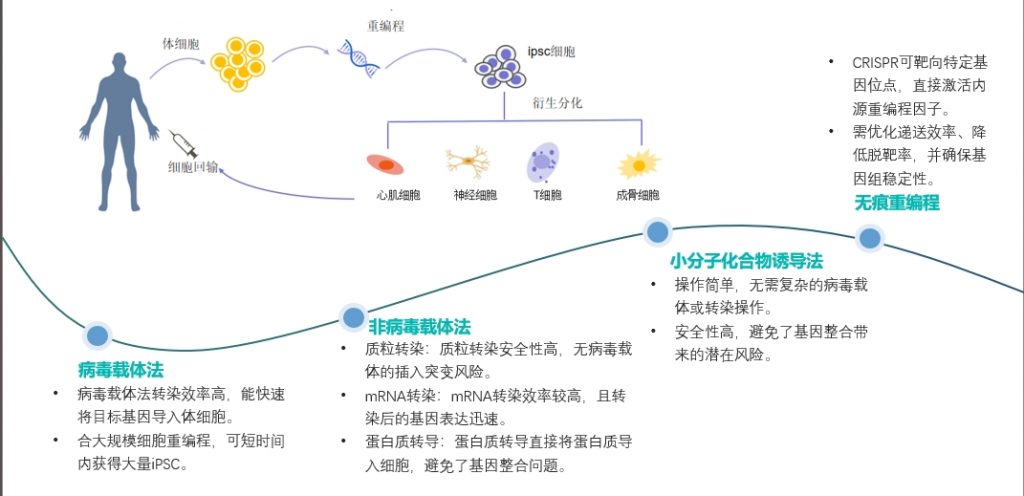
(图3:iPSC不同的重编程方法)
在加州大学洛杉矶分校的实验室里,神经科学家Clive Svendsen正用渐冻症患者的iPSC构建运动神经元模型。这些在培养皿中逐渐僵化的细胞,忠实地复现了疾病进程,使新药研发周期从10年缩短至18个月。而在大洋彼岸,京都大学的眼科医生西田幸二,已为200多名角膜损伤患者移植了iPSC培育的角膜组织,其中一位80岁的老人在术后首次看清孙女的毕业证书时,泪水浸透了纱布。
这仅是冰山一角:帕金森病药物在iPSC模型中的筛选准确率已达92%;基于患者特异性iPSC的个性化疫苗进入Ⅱ期临床;通过重编程技术,90岁老人的皮肤细胞被逆转至胚胎状态;在加州IPSC细胞库里保存着科技富豪们价值百万美元的“青春备份”——他们年轻时储存的iPSC, 随时可被分化为年轻器官和组织细胞。
超越医学:重塑文明的生物革命
iPSC技术的意义,早已超越疾病治疗本身。它改写了“细胞命运不可逆”的生命定律,证明60万亿个人体细胞都蕴藏着“重生”的密码。当个性化医疗从“精准用药”升级为“再造器官”,当90岁老人的细胞能与新生儿同样年轻,人类对生老病死的认知将被彻底颠覆。
iPSC可从患者自身血液、皮肤组织获取体细胞进行iPSC重编程,为大规模细胞治疗提供了可能;具有无限自我更新能力,可在体外长期培养并保持稳定状态;大量扩增iPSC后分化为几乎所有类型的细胞,可根据疾病类型和治疗需求,定向分化为特定功能细胞,为治疗各种疾病提供可能。iPSC的特点决定了其巨大的应用潜力,也让iPSC储存成为人们寻找健康与长寿的一条新路径。
全球最大的iPSC资源库——加州再生医学研究所,成立于2004年,得到美国加州第71号提案批准,获得30亿美元资金支持,是加利福尼亚州政府设立的一个机构,旨在加速干细胞治疗产品的开发和应用,以解决医学难题?。除此以外,全球已有23个国家建立商业级iPSC存储库,iPSC存储正从科研设施走向商业服务,从药物研发走向个性化治疗。2024年市场数据显示全球商业存储市场规模达23亿美元,中国占比38%增速第一。

(图4:加州再生医学研究所,California institute for regenerative medicine)
2025年2月24日,美国剑桥市的细胞科技公司Cellino与麻省总医院布莱根基因和细胞治疗研究所(GCTI)宣布,联合启动全球首个基于医院的自体诱导多能干细胞 (iPSC)制备中心。
在这场静默的革命中,中国既是追赶者,更是引领者。北京、深圳、上海等地建立的iPSC细胞库,已存储超过10万例疾病模型;2025年4月,海南省也在科技的热潮中悄悄发力,海南济民博鳌国际医院引进美国加州大学研究团队筹建中国第一个医院级自体诱导多能干细胞 (iPSC)制备中心及iPSC银行。与传统iPSC制备需数月相比,医院内集成化生产可将周期压缩至数周,满足急性疾病需求。同时,利用医院平台和资源可加速基础研究与临床医学的融合,加速临床研究落地与技术转化。
正如《科学》杂志所言:“iPSC不仅是一场医学革命,更是一个民族在生物科技赛道上的战略支点。”
结语:普罗米修斯的新火种
从古希腊神话到现代实验室,人类对生命奥秘的探索从未停歇。iPSC技术就像新时代的火种,照亮了再生医学的幽深隧道。当科学家们像程序员调试代码般修改细胞命运时,我们或许正在见证文明史上最深刻的转折——那个能自主修复生命、逆转时光的未来,正从论文中的字符,一步步变成诊室里的奇迹。